Chế biến magiê, chuẩn bị quặng magiê để sử dụng trong các sản phẩm khác nhau.

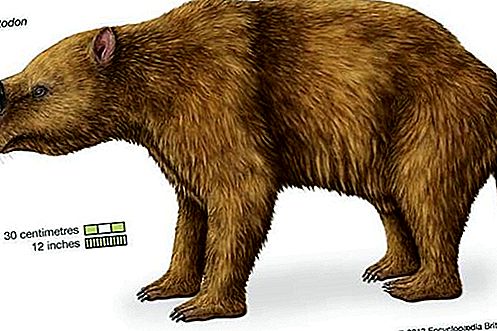
Magiê (Mg) là một kim loại màu trắng bạc có bề ngoài tương tự như nhôm nhưng nặng hơn một phần ba. Với mật độ chỉ 1.738 gram trên mỗi cm khối, nó là kim loại cấu trúc nhẹ nhất được biết đến. Nó có cấu trúc tinh thể đóng kín hình lục giác (hcp), do đó, giống như hầu hết các kim loại của cấu trúc này, nó thiếu độ dẻo khi làm việc ở nhiệt độ thấp hơn. Ngoài ra, ở dạng nguyên chất, nó thiếu đủ sức mạnh cho hầu hết các ứng dụng kết cấu. Tuy nhiên, việc bổ sung các nguyên tố hợp kim giúp cải thiện tính chất của nó đến mức cả hợp kim magiê đúc và rèn được sử dụng rộng rãi, đặc biệt khi trọng lượng nhẹ và cường độ cao là quan trọng.
Magiê phản ứng mạnh với oxy ở nhiệt độ cao; trên 645 ° C (1.190 ° F) trong không khí khô, nó cháy với ánh sáng trắng sáng và nhiệt độ cao. Vì lý do này, bột magiê được sử dụng trong pháo hoa. Ở nhiệt độ phòng, một màng ổn định của magiê hydroxit không tan trong nước hình thành trên bề mặt kim loại, bảo vệ nó khỏi bị ăn mòn trong hầu hết các khí quyển. Là một chất phản ứng mạnh tạo thành các hợp chất ổn định với clo, oxy và lưu huỳnh, magiê có một số ứng dụng luyện kim, như trong sản xuất titan từ titan tetrachloride và trong quá trình khử lưu huỳnh của sắt lò cao. Phản ứng hóa học của nó cũng được thấy rõ trong các hợp chất magiê có ứng dụng rộng rãi trong công nghiệp, y học và nông nghiệp.
Lịch sử
Magiê có tên từ magnesit, một khoáng chất magiê carbonate, và lần lượt khoáng chất này được cho là có tên của nó với các trầm tích magnesit được tìm thấy ở Magnesia, một huyện thuộc vùng Hy Lạp cổ đại của Hy Lạp. Nhà hóa học người Anh Humphry Davy được cho là đã sản xuất một hỗn hợp magiê vào năm 1808 bằng cách điện phân magiê sunfat ẩm, sử dụng thủy ngân làm cực âm. Tuy nhiên, magiê kim loại đầu tiên được sản xuất vào năm 1828 bởi nhà khoa học người Pháp A.-A.-B. Bussy. Công việc của ông liên quan đến việc giảm magiê clorua nóng chảy bằng kali kim loại. Năm 1833, nhà khoa học người Anh Michael Faraday là người đầu tiên sản xuất magiê bằng cách điện phân magiê clorua nóng chảy. Các thí nghiệm của ông đã được lặp lại bởi nhà hóa học người Đức Robert Bunsen.
Sản xuất công nghiệp thành công đầu tiên được bắt đầu ở Đức vào năm 1886 bởi Aluminium Magiêfabrik Hemelingen, dựa trên sự điện phân của Carnallite nóng chảy. Hemelingen sau đó trở thành một phần của tổ hợp công nghiệp IG Farbenindustrie, trong những năm 1920 và 30, đã phát triển một quy trình sản xuất một lượng lớn magiê clorua nóng chảy và chủ yếu là nước (hiện được gọi là quy trình IG Farben) cũng như công nghệ để điện phân sản phẩm này thành kim loại magiê và clo. Những đóng góp khác của IG Farben là sự phát triển của nhiều hợp kim đúc và dễ uốn, thông lượng tinh chế và bảo vệ, các sản phẩm magiê rèn, và một số lượng lớn các ứng dụng máy bay và ô tô. Trong Thế chiến II, Công ty Hóa chất Dow của Hoa Kỳ và Magiê Elektron Limited của Vương quốc Anh đã bắt đầu giảm magiê điện phân từ nước biển được bơm từ Vịnh Galveston, Texas và Biển Bắc tại Hartlepool, Anh. Đồng thời tại Ontario, Canada, quy trình khử oxit magiê bằng silic bằng silicon trong các lò phản ứng bắn ra bên ngoài đã được giới thiệu.
Sau chiến tranh, các ứng dụng quân sự mất đi sự nổi bật. Dow Chemical mở rộng thị trường dân sự bằng cách phát triển các sản phẩm rèn, công nghệ photoeng giác và hệ thống xử lý bề mặt. Khai thác vẫn dựa trên điện phân và giảm nhiệt. Các quy trình này đã được thực hiện các tinh chỉnh như gia nhiệt bên trong các vặn lại (quy trình Magnetherm, được giới thiệu ở Pháp vào năm 1961), chiết xuất từ các chất magiê clorua khử nước (do công ty Norsk Hydro của Na Uy giới thiệu năm 1974) và cải tiến công nghệ tế bào điện phân từ năm 1974) khoảng năm 1970.
Tính đến năm 2019, Trung Quốc đã sản xuất khoảng 85% magiê của thế giới và Nga, Kazakhstan, Israel và Brazil đã sản xuất phần lớn còn lại.
Quặng và nguyên liệu
Nguyên tố phổ biến thứ tám trong tự nhiên, magiê chiếm 2,4% vỏ Trái đất. Do tính phản ứng mạnh của nó, nó không xảy ra ở trạng thái tự nhiên, mà nó được tìm thấy trong rất nhiều hợp chất trong nước biển, nước muối và đá.
Trong số các khoáng vật quặng, phổ biến nhất là dolomit carbonat (một hợp chất của magiê và canxi cacbonat, MgCO 3 · CaCO 3) và magnesit (magiê carbonate, MgCO 3). Ít phổ biến hơn là khoáng chất hydroxit brucite, Mg (OH) 2 và Carnallite khoáng chất halide (một hợp chất của magiê và kali clorua và nước, MgCl 2 · KCl · 6H 2 O).
Magiê clorua có thể phục hồi từ các loại nước muối tự nhiên như Great Salt Lake (thường chứa 1,1% khối lượng magiê) và Biển Chết (3,4%), nhưng cho đến nay, nguồn lớn nhất là các đại dương trên thế giới. Mặc dù nước biển chỉ xấp xỉ 0,13% magiê, nhưng nó đại diện cho một nguồn gần như không cạn kiệt.
Khai thác và tập trung
Cả dolomite và magnesite đều được khai thác và cô đặc bằng các phương pháp thông thường. Carnallite được đào dưới dạng quặng hoặc tách ra khỏi các hợp chất muối khác được đưa lên bề mặt bằng cách khai thác giải pháp. Nước muối có chứa magiê tự nhiên được tập trung trong các ao lớn bằng cách bốc hơi mặt trời.
Khai thác và tinh chế
Một thuốc thử hóa học mạnh, magiê tạo thành các hợp chất ổn định và phản ứng với oxy và clo ở cả trạng thái lỏng và khí. Điều này có nghĩa là khai thác kim loại từ nguyên liệu thô là một quá trình tốn nhiều năng lượng đòi hỏi các công nghệ được điều chỉnh tốt. Sản xuất thương mại tuân theo hai phương pháp hoàn toàn khác nhau: điện phân magiê clorua hoặc khử nhiệt oxit magiê thông qua quy trình Pidgeon. Điện phân từng chiếm khoảng 75% sản lượng magiê thế giới. Tuy nhiên, vào đầu thế kỷ 21, khi Trung Quốc nổi lên là nhà sản xuất magiê hàng đầu thế giới, chi phí lao động và năng lượng thấp cho phép quá trình Pidgeon có hiệu quả kinh tế mặc dù kém hiệu quả hơn so với điện phân.
Điện phân
Các quá trình điện phân bao gồm hai bước: điều chế nguyên liệu có chứa magiê clorua và phân ly hợp chất này thành kim loại magiê và khí clo trong các tế bào điện phân.
Trong các quy trình công nghiệp, thức ăn tế bào bao gồm các loại muối nóng chảy khác nhau có chứa magiê clorua khan (chủ yếu là không có nước), magiê clorua mất nước một phần hoặc Carnallite khan. Để tránh các tạp chất có trong quặng Carnallite, Carnallite nhân tạo khử nước được tạo ra bằng cách kết tinh có kiểm soát từ các dung dịch chứa magiê và kali nóng. Magiê clorua khử nước một phần có thể thu được bằng quá trình Dow, trong đó nước biển được trộn trong chất keo tụ với dolomit phản ứng cháy nhẹ. Một magiê hydroxit không hòa tan kết tủa vào đáy bể lắng, từ đó nó được bơm dưới dạng bùn, được lọc, chuyển thành magiê clorua bằng phản ứng với axit hydrochloric và làm khô trong một loạt các bước bay hơi đến 25% lượng nước. Mất nước cuối cùng diễn ra trong quá trình nấu chảy.
Clorua magiê khan được sản xuất bằng hai phương pháp chính: khử nước magiê clorua hoặc clo hóa oxit magiê. Trong phương pháp thứ hai, được minh họa bằng quy trình IG Farben, dolomit bị đốt cháy nhẹ được trộn với nước biển trong chất keo tụ, trong đó magiê hydroxit được kết tủa, lọc và nung thành oxit magiê. Điều này được trộn với than củi, tạo thành các viên với việc bổ sung dung dịch magiê clorua và sấy khô. Các hạt được tích điện vào một chất khử clo, lò nung lót gạch, nơi chúng được đốt nóng bằng các điện cực carbon đến khoảng 1.000 Lời1,200 ° C (1.800 Lời2,200 ° F). Khí clo được đưa vào qua các cửa sổ trong lò phản ứng với oxit magiê để tạo ra magiê clorua nóng chảy, được gõ vào các khoảng thời gian và gửi đến các tế bào điện phân.
Mất nước của magiê nước muối được tiến hành trong các giai đoạn. Trong quy trình Norsk Hydro, tạp chất trước tiên được loại bỏ bằng cách kết tủa và lọc. Nước muối tinh khiết, chứa khoảng 8,5 phần trăm magiê, được cô đặc bằng cách bay hơi đến 14 phần trăm và chuyển đổi thành các hạt trong một tháp prilling. Sản phẩm này được sấy khô thêm cho các hạt không có nước và chuyển đến các tế bào điện phân.
Các tế bào điện phân về cơ bản là các tàu lót gạch được trang bị nhiều catốt thép và cực dương than chì. Chúng được gắn theo chiều dọc thông qua nắp tế bào và ngập một phần trong chất điện phân muối nóng chảy bao gồm clorua kiềm mà magiê clorua tạo ra trong các quy trình được mô tả ở trên được thêm vào ở nồng độ 6 đến 18 phần trăm. Phản ứng cơ bản là:
Nhiệt độ hoạt động thay đổi từ 680 đến 750 ° C (1.260 đến 1.380 ° F). Tiêu thụ điện năng là 12 đến 18 kilowatt-giờ cho mỗi kg magiê được sản xuất. Clo và các loại khí khác được tạo ra ở cực dương than chì và kim loại magiê nóng chảy nổi lên trên đỉnh của bể muối, nơi nó được thu thập. Clo có thể được tái sử dụng trong quá trình khử nước.
Giảm nhiệt
Trong sản xuất nhiệt, dolomite được nung thành magiê oxit (MgO) và vôi (CaO), và chúng được khử bằng silic (Si), thu được khí magiê và một xỉ silicat dicalcium. Phản ứng cơ bản, Đó là nhiệt độ nhiệt, nghĩa là, nhiệt phải được áp dụng để bắt đầu và duy trì nó. Với magiê đạt áp suất hơi 100 kilopascals (1 khí quyển) ở 1.800 ° C (3.270 ° F), yêu cầu nhiệt có thể khá cao. Để giảm nhiệt độ phản ứng, các quá trình công nghiệp hoạt động trong chân không. Có ba phương pháp chính, khác nhau bởi phương tiện cung cấp nhiệt. Trong quy trình Pidgeon, dolomit nghiền và nung được trộn với ferrosilicon nghiền mịn, đóng bánh, và tích điện vào các vấu thép-niken-crom hình trụ. Một số vặn lại được lắp đặt theo chiều ngang trong lò đốt dầu hoặc khí đốt, có nắp đậy và hệ thống ngưng tụ kèm theo kéo dài ra khỏi lò. Sau một chu kỳ phản ứng ở nhiệt độ 1.200 ° C (2.200 ° F) và dưới áp suất giảm 13 pascal, các tinh thể magiê (được gọi là vương miện) được loại bỏ khỏi thiết bị ngưng tụ, xỉ được sơ tán dưới dạng chất rắn và vặn lại được nạp lại. Trong quy trình Bolzano, than bánh dolomit-ferrosilicon được xếp chồng lên nhau trên một hệ thống hỗ trợ điện tích đặc biệt thông qua đó đốt nóng điện bên trong được thực hiện để tích điện. Một phản ứng hoàn toàn mất 20 đến 24 giờ ở 1.200 ° C dưới 400 pascal.
Xỉ silicat dicalcium được sản xuất bởi các quá trình trên có nhiệt độ nóng chảy khoảng 2.000 ° C (3.600 ° F) và do đó xuất hiện dưới dạng chất rắn, nhưng, bằng cách thêm alumina (nhôm oxit, Al 2 O 3) vào điện tích, điểm nóng chảy có thể giảm xuống còn 1.550 trừ1.600 ° C (2.825 trừ2.900 ° F). Kỹ thuật này, được sử dụng trong quy trình Magnetherm, có ưu điểm là xỉ lỏng có thể được làm nóng trực tiếp bằng dòng điện thông qua điện cực đồng làm mát bằng nước. Phản ứng khử xảy ra ở 1.600 ° C và áp suất 400 pao670 pascal. Magiê bay hơi được ngưng tụ trong một hệ thống riêng biệt gắn liền với lò phản ứng, và xỉ nóng chảy và ferrosilicon được gõ trong khoảng thời gian.