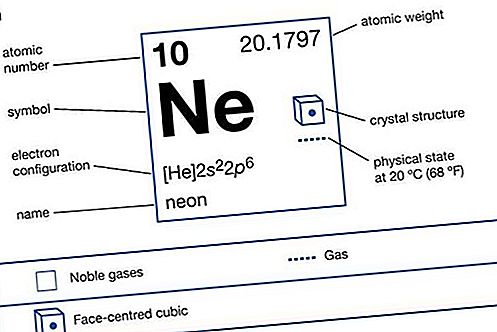
Neon (Ne), nguyên tố hóa học, khí trơ thuộc nhóm 18 (khí hiếm) của bảng tuần hoàn, được sử dụng trong các dấu hiệu điện và đèn huỳnh quang. Không màu, không mùi, không vị và nhẹ hơn không khí, khí neon xuất hiện với số lượng nhỏ trong bầu khí quyển của Trái đất và bị mắc kẹt trong lớp đá của vỏ Trái đất. Mặc dù neon là khoảng 3 1 / 2 lần dồi dào như heli trong khí quyển, không khí khô chỉ chứa 0,0018 trăm neon theo thể tích. Yếu tố này có nhiều trong vũ trụ hơn trên Trái đất. Hóa lỏng Neon tại -246,048 ° C (-411 ° F) và đóng băng ở nhiệt độ chỉ có 2 1 / 2° thấp hơn. Khi ở dưới áp suất thấp, nó sẽ phát ra ánh sáng đỏ cam rực rỡ nếu một dòng điện được truyền qua nó. Đặc tính này được sử dụng trong các dấu hiệu neon (lần đầu tiên trở nên quen thuộc vào những năm 1920), trong một số đèn dẫn huỳnh quang và khí, và trong các máy thử điện áp cao. Tên neon có nguồn gốc từ tiếng Hy Lạp neos, mới.

khí hiếm
là helium (He), neon (Ne), argon (Ar), krypton (Kr), xenon (Xe), radon (Rn), và oganesson (Og). Các khí cao quý là không màu, không mùi,
Neon được phát hiện (1898) bởi các nhà hóa học người Anh Sir William Ramsay và Morris W. Travers là một thành phần của phần dễ bay hơi nhất của argon thô hóa lỏng thu được từ không khí. Nó ngay lập tức được công nhận là một yếu tố mới bởi ánh sáng độc đáo của nó khi được kích thích bằng điện. Nguồn thương mại duy nhất của nó là bầu khí quyển, trong đó nó là 18 phần triệu. Vì nhiệt độ sôi của nó là −246 ° C (411 ° F), neon vẫn còn, cùng với heli và hydro, trong một phần nhỏ của không khí chống lại sự hóa lỏng khi làm lạnh đến −195,8 ° C (−320,4 ° F, điểm sôi của nitơ lỏng). Neon được phân lập từ hỗn hợp khí lạnh này bằng cách đưa nó tiếp xúc với than hoạt tính, chất hấp phụ neon và hydro; loại bỏ hydro được thực hiện bằng cách thêm đủ oxy để chuyển đổi tất cả thành nước, cùng với bất kỳ oxy dư thừa, ngưng tụ khi làm mát. Xử lý 88.000 pound không khí lỏng sẽ tạo ra một pound neon.
Không có hợp chất hóa học ổn định của neon đã được quan sát. Các phân tử của nguyên tố bao gồm các nguyên tử đơn. Neon tự nhiên là hỗn hợp của ba đồng vị bền: neon-20 (90,92 phần trăm); neon-21 (0,26 phần trăm); và neon-22 (8,82 phần trăm). Neon là nguyên tố đầu tiên được hiển thị bao gồm nhiều hơn một đồng vị ổn định. Năm 1913, ứng dụng kỹ thuật quang phổ khối cho thấy sự tồn tại của neon-20 và neon-22. Đồng vị ổn định thứ ba, neon-21 được phát hiện sau đó. Mười hai đồng vị phóng xạ của neon cũng đã được xác định.
Thuộc tính nguyên tố
| số nguyên tử | 10 |
|---|---|
| trọng lượng nguyên tử | 20.183 |
| độ nóng chảy | 48248,67 ° C (−415,5 ° F) |
| điểm sôi | −246.048 ° C (−411 ° F) |
| mật độ (1 atm, 0 ° C) | 0,89990 g / lít |
| trạng thái oxy hóa | 0 |
| cấu hình electron. | 1s 2 2s 2 2p 6 |